پیری یکی از پیچیدهترین فرآیندهای زیستی است که تحت تأثیر مجموعهای از عوامل ژنتیکی، محیطی و اپیژنتیکی قرار دارد. در سالهای اخیر، مفهوم اپی ژنتیک در پیری توجه گستردهای را به خود جلب کرده است. اپیژنتیک به تغییرات ارثی در بیان ژنها اشاره دارد که بدون تغییر در توالی DNA رخ میدهد. این تغییرات شامل متیلاسیون DNA، تغییرات در هیستونها و تنظیم توسط RNAهای غیرکُدکننده هستند. پژوهشها نشان دادهاند که با افزایش سن، الگوهای اپیژنتیکی در سلولها دستخوش تغییر میشوند و همین امر نقش اساسی در بروز علائم و بیماریهای وابسته به پیری دارد (اگر به این موارد علاقه دارید، می توانید مقاله چرا غربالگری روانی در سالمندان باید انجام شود؟ را مطالعه کنید).
فهرست مطالب
مفهوم اپیژنتیک و ارتباط آن با پیری

اصطلاح اپیژنتیک نخستینبار توسط کنراد وادینگتون در دههی ۱۹۴۰ معرفی شد. وی آن را بهعنوان «تعامل بین ژنها و محیط» تعریف کرد. در سلولهای انسانی، DNA در اطراف پروتئینهایی به نام هیستون پیچیده است. تغییرات شیمیایی در DNA یا هیستونها میتواند باعث فعال یا غیرفعال شدن ژنها شود. در فرآیند اپی ژنتیک در پیری، این تغییرات بهصورت تجمعی رخ داده و منجر به کاهش کارایی سلول، بروز التهاب مزمن و افزایش خطر ابتلا به بیماریهایی مانند سرطان و آلزایمر میشود.
تغییرات متیلاسیون DNA در طول پیری
متیلاسیون DNA یکی از مهمترین مکانیسمهای اپیژنتیکی است. در جوانی، الگوی متیلاسیون نسبتاً پایدار است، اما با گذر زمان، این الگو تغییر میکند. کاهش متیلاسیون در برخی نواحی ژنومی باعث فعال شدن ژنهای نامطلوب میشود، در حالی که افزایش متیلاسیون در ژنهای تنظیمی ممکن است عملکرد طبیعی سلول را مختل کند. دانشمندان با بررسی این الگوها توانستهاند «ساعت اپیژنتیکی» را توسعه دهند که سن بیولوژیکی افراد را با دقت بالایی تخمین میزند. این ابزار نشان میدهد که اپی ژنتیک در پیری نهتنها نتیجهی گذر زمان، بلکه نتیجهی سبک زندگی و مواجههی محیطی نیز هست.
تغییرات هیستونی و بازسازی کروماتین
در کنار متیلاسیون، تغییرات در ساختار هیستونها نیز نقش اساسی در اپی ژنتیک در پیری دارند. هیستونها با افزودن یا حذف گروههای شیمیایی مانند استیل، متیل یا فسفات، میتوانند بیان ژن را تنظیم کنند. با افزایش سن، تعادل میان این تغییرات از بین میرود و دسترسی ژنها به ماشین رونویسی دچار اختلال میشود. این امر در نهایت منجر به ناپایداری ژنومی، افزایش جهشها و کاهش بازسازی بافتها میگردد.
RNAهای غیرکدکننده و نقش آنها در پیری
RNAهای غیرکدکننده مانند microRNA و lncRNA در تنظیم اپیژنتیک ژنها مشارکت دارند. آنها با مهار یا فعالسازی ترجمهی mRNAها، بیان ژنها را بهشکل ظریفی تنظیم میکنند. مطالعات اخیر نشان دادهاند که در روند اپی ژنتیک در پیری، برخی microRNAها دچار تغییر بیان میشوند. بهعنوان نمونه، افزایش miR-34a با کاهش بازسازی سلولی و تسریع پیری بافتی مرتبط است.
عوامل محیطی مؤثر بر اپی ژنتیک در پیری
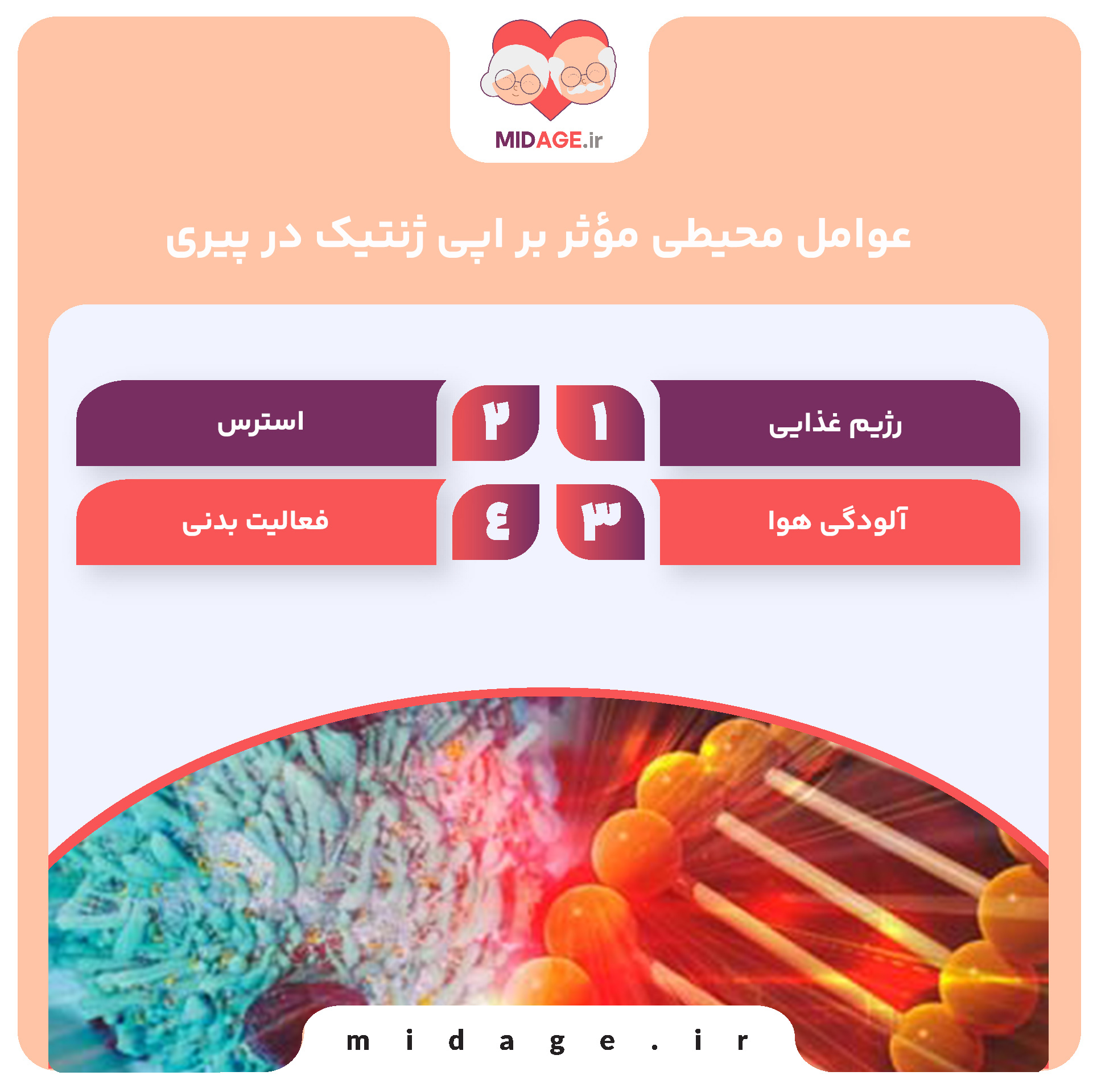
عوامل متعددی از جمله رژیم غذایی، استرس، آلودگی هوا و فعالیت بدنی بر الگوهای اپیژنتیکی تأثیر میگذارند. رژیمهای سرشار از آنتیاکسیدان و ویتامینهای گروه B میتوانند الگوهای متیلاسیون را بهبود بخشند، در حالی که استرس مزمن سبب تسریع تغییرات اپیژنتیکی نامطلوب میشود. ورزش منظم یکی از راهکارهای مؤثر در تعدیل اپی ژنتیک در پیری محسوب میشود، زیرا موجب افزایش استیلاسیون هیستونها و بهبود عملکرد میتوکندری میگردد.
جدول: نمونههایی از تغییرات اپیژنتیکی مرتبط با پیری
| نوع تغییر اپیژنتیکی | اثر بر بیان ژن | نتیجهی فیزیولوژیکی | نمونهی بیماری مرتبط |
| کاهش متیلاسیون در نواحی تکراری DNA | افزایش بیان ژنهای بیثباتکننده ژنوم | ناپایداری ژنتیکی | سرطانها |
| افزایش متیلاسیون پروموتر ژنهای سرکوبگر تومور | خاموشی ژنهای محافظ | افزایش خطر تومورزایی | سرطان کولورکتال |
| تغییر در استیلاسیون هیستون H3 | اختلال در دسترسی کروماتین | کاهش رونویسی ژنهای ترمیمی | پیری سلولی |
| افزایش بیان miR-34a | مهار مسیرهای بازسازی سلول | کاهش توان ترمیم بافت | فیبروز و زوال عصبی |
| کاهش lncRNAهای حفاظتی | از بین رفتن پایداری ژنومی | تسریع پیری سیستمیک | بیماری آلزایمر |
این جدول بهخوبی نشان میدهد که چگونه تغییرات اپیژنتیکی در سطح مولکولی میتوانند منجر به تغییرات فیزیولوژیکی مرتبط با پیری شوند.
اپی ژنتیک در پیری و بیماریهای وابسته به سن
یکی از نتایج برجستهی پژوهشها این است که الگوهای اپیژنتیکی تغییریافته با بیماریهای مزمن مرتبط با سن ارتباط مستقیم دارند. برای مثال، در بیماران آلزایمر، کاهش متیلاسیون ژنهای خاصی مشاهده شده که منجر به تجمع پروتئینهای سمی در مغز میشود. در دیابت نوع دوم نیز تغییرات اپیژنتیکی در ژنهای متابولیسم گلوکز دیده میشود. بنابراین، درک مکانیسمهای اپی ژنتیک در پیری میتواند مسیرهای درمانی جدیدی را برای پیشگیری از این بیماریها آشکار سازد.
بازگرداندن تغییرات اپیژنتیکی
یکی از جذابترین یافتهها در سالهای اخیر این است که برخی تغییرات اپیژنتیکی برگشتپذیرند. مطالعات بر روی حیوانات نشان دادهاند که با استفاده از داروهای تنظیمکنندهی اپیژنتیک مانند مهارکنندههای متیلاسیون DNA، میتوان روند پیری سلولی را کند کرد. همچنین، بازبرنامهریزی سلولهای پیر از طریق فاکتورهای یاماناکا باعث بازگشت الگوهای جوانی در DNA شده است. این شواهد تأکید میکند که اپی ژنتیک در پیری نهتنها یک فرآیند اجتنابناپذیر، بلکه قابل مداخله و حتی قابل بازسازی است.
اپی ژنتیک در پیری و پزشکی شخصی
با پیشرفت فناوریهای تعیین توالی و تحلیل بیوانفورماتیکی، امکان بررسی دقیق الگوهای اپیژنتیکی هر فرد فراهم شده است. این دادهها میتوانند برای طراحی برنامههای شخصی تغذیه، ورزش و درمان دارویی بهکار روند. در آینده، ممکن است پزشکان بر اساس «ساعت اپیژنتیکی» هر فرد، درمانهای ضدپیری را تنظیم کنند. بنابراین، اپی ژنتیک در پیری میتواند به یکی از پایههای اصلی پزشکی دقیق (Precision Medicine) تبدیل شود.
نتیجهگیری
در مجموع، پیری نهتنها پیامد گذر زمان، بلکه نتیجهی تغییرات عمیق در سطح اپیژنتیکی است. این تغییرات بیان ژن را تحت تأثیر قرار داده و منجر به کاهش عملکرد سلولها، بروز التهاب مزمن و افزایش خطر بیماریهای وابسته به سن میشوند. با این حال، امیدواری زیادی وجود دارد که با درک بهتر سازوکارهای اپی ژنتیک در پیری بتوان راهکارهایی برای کند کردن یا حتی معکوس کردن این فرآیند یافت.













ارسال پاسخ
نمایش دیدگاه ها